国药集团武汉血液制品有限公司招标公告
本公司因生产需要,对血液制剂室后处理车间需要的250L移动罐进行公开招标,欢迎具有相应资质的单位前来报名投标。
招标内容:国药集团武汉血液制品有限公司250L移动罐
1.目的
本URS是一份用于定义血液制剂室250L 移动罐的选型方法、功能要求、关键参数等的关键文件。用于指导选型,单位按照我公司的相关要求并结合相关规范进行设计、安装及后期验证等一系列工作。
2.范围
本URS仅用于国药集团武汉血液制品有限公司血液制剂室250L移动罐的购买。
3.职责
|
部 门 |
职 责 |
|
血液制剂室 |
负责从用户的角度起草并审核本URS文件。
负责本URS文件的修改、打印,并将纸质版送各相关部门签字。 |
|
工程运行室 |
负责从项目施工角度审核本URS文件。
负责补充项目施工相关内容。 |
|
负责从工程技术角度审核本URS文件。
负责补充工程技术及维护维修相关内容。
负责本URS文件归档。 |
|
生产技术部 |
负责从生产技术角度审核本URS文件。 |
|
质量保证部 |
负责提供URS文件模板。
负责从质量管理法规角度审核本URS文件。
负责批准本URS文件。 |
4.内容
4.1概述
血液制剂室后处理生产车间需要购买250L移动罐20台。250L 移动罐是除菌后制品的装载容器。保证制品原液在生产过程中的标准化储存密封和安全方便的移动。
4.2法规要求
4.2.1 GMP要求
4.2.1.1《药品生产质量管理规范》(现行版)
4.2.1.2《药品GMP指南》无菌药品(现行版)
本设备所包含的罐体及管道、配件、 阀门用材符合cGMP&EU-GMP规范要求。
4.2.2安全及环保要求
4.2.2.1本设备按GB150-1998、HG20584-98、等相关标准设计、制造、 检验和验收、并接受核压力容器安全技术监察规程的监督。
4.2.2.2焊接探伤JB/T4730.1-4730.6-2005标准进行评定,III级合格证,探伤比例不少于20%。
4.2.3其他要求
N/A
4.3安装要求
4.3.1 安装位置
血液制剂大楼二层后处理生产车间
4.3.2安装尺寸
N/A
4.3.4地面承重
N/A
4.3.5可用的公用系统
N/A
4.3.6洁净级别及房间环境条件
4.3.6.1洁净级别为A级控制区。
4.3.6.2环境温度:18℃-25℃以下。
4.3.6.3环境湿度:45%RH-65%RH
4.3.7可用的能源配置
N/A
4.3.8外观及材质要求
4.3.8.1移动罐外观应光滑整洁无清洁死角。罐内电抛光Ra≤0.4um,无死角方便清洁卫生;罐体外表面机械抛光达亚光,抛光Ra≤0.8um;
4.3.8.2此容器为单层立式压力容器;罐体采用双碟型封头,配有隔膜压力表、 温度表、 呼吸器、 清洗器、 罐底阀等附件,罐内无死角,方便清洁罐内。
4.3.8.3罐底出口到地面的距离≥350mm,罐内扩物料过流和接触部件的材料采用SUS316L不锈钢,其余材料采用SUS304不锈钢。
4.3.8.4所有接口均为标准快装式接口
4.3.8.5移动罐需配有脚轮,方便移动。
4.3.9其他安装要求
N/A
4.4运行要求
4.4.1原辅料、包装材料、产品的规格标准
4.4.2设备效率、产能
4.4.3工艺参数范围
4.4.3.1设计压力:0.4MPa;
4.4.3.2工作压力:0.3MPa;
4.4.3.3设计温度:150°C;
4.4.3.4工作温度:0-121°C。
4.4.3.5公称容积:250L;装料系数:85%
4.4.4性能要求
4.4.4.1
移动罐制造厂家不生产,需从其他制造厂家购买的主要零部件:
|
零部件名称 |
数量 |
生产厂家 |
|
温度探头 |
1 |
进口 |
|
可拆卸罐体隔膜阀(进料,出料) |
2 |
盖米 |
|
安全阀 |
1 |
斯派莎克 |
|
疏水性呼吸器 |
1 |
millpore |
|
隔膜压力表 |
1 |
进口 |
|
喷淋球 |
1 |
进口 |
4.4.4.2加工制造要求:a,需要焊接的部位采用氩弧焊:SUS316L选用HOOCr9Ni12Mo2焊丝,SUS304选用HOCr21Ni10焊丝。b,筒仃对接的A,B类焊缝经外观检查合格后,进行X射线检测,其检测长度不得小于各条焊缝长度的20%,检测结果按JB/T4730.1—4730.6—2005标准进行评定,III级合格。c,容器完工后,与物料接触面均应酸洗、钝化处理。e,使用材料表面应无裂纹、划伤凹坑,麻点等缺陷存在。
4.4.4.3全封闭设计,可进行CIP和SIP,符合FDA和GMP的要求。
4.4.5其他运行要求
4.4.5.1需配备观察窗并能观察制品外观与性状,罐体有带刻度的观察窗可确认罐内容积。
4.4.5.2需跟原型号 YDG 250移动罐的配件通用。
4.5电气、自动控制要求
4.5.1自动控制过程的要求
N/A
4.5.2计算机化系统的验证要求
N/A
4.5.3其他要求
N/A
4.6安全要求
4.6.1密封连锁及压力保护
移动罐组装完毕后,以水带料试运行。本设备包含的盲板、堵头等部件应安装在设备上一起试压(或试漏),并和设备一起发运。(要求所有部件能轻松安装)。
4.6.2电气保护
N/A
4.6.3其他要求
N/A
4.7文件要求
4.7.1提供技术文件包含:产品合格证;使用说明书;压力容器鉴检书;装箱单;易损件、 配件、 专用工具清单及易损件五年内价格清单。
设备所有材料 零部件全部原始资料,包括说明书 材料证明书 合格证;计量检测元器件 安全附件仪器仪表等要求出具出厂时国家有关部门的校验报告。
4.7.2 CE认证服务及证书。
4.8服务要求
4.8.1培训要求
投标方负责培训本设备操作、维修人员技术培训。
4.8.2运输要求
投标方将设备送至购方现场(武汉市江夏区郑店街黄金村106大楼二层后处理区),罐体运输应防止运输、搬运过程中对罐体的损伤、并能要求能有效的保持罐体内外清洁。并派专业人员安装调试(具体时间到货后,听购方通知)
4.8.3验证要求
4.8.3.1投标方按GMP规范完成DQ、IQ、OQ、PQ工作,并提供相应文件。
4.8.3.2投标方负责设备安装性能验证,出具验证报告书并制定设备操作、维护保养SOP。
4.8.4售后服务及备件要求
4.8.4.1供应商国内应设有备件库,能够及时提供所有备件:基本配件随时可发货,特殊配件最长不超过2周到货。
4.8.4.2设备保质期从确认验收的阶段开始计算,设备质保期为一年,一年内免费保修,一年后应提供良好的售后服务。
4.8.4.3售后服务必须响应及时,要求设备出现须厂家维修的故障后,应在4小时内明确答复,当电话沟通无法解决时,须24小时内派人至现场解决。
4.8.5验收要求
4.8.5.1投标方应根据上述要求提出方案图纸,并满足cGMP和EU-GMP相关要求。方案图纸及设备加工图纸需招标方相关技术人员签字确认后方可实施。
4.8.5.2到货时,由QA、采购储运室、工程运行室、供货商、四方当场开箱验货,对250L 移动罐和配件进行核对,并由生产厂家提供验收报告。
4.8.5.4验收时发现设备对URS的响应不完全,甲方有权利拒绝验收。
5.附件
5.1 移动罐样式图:
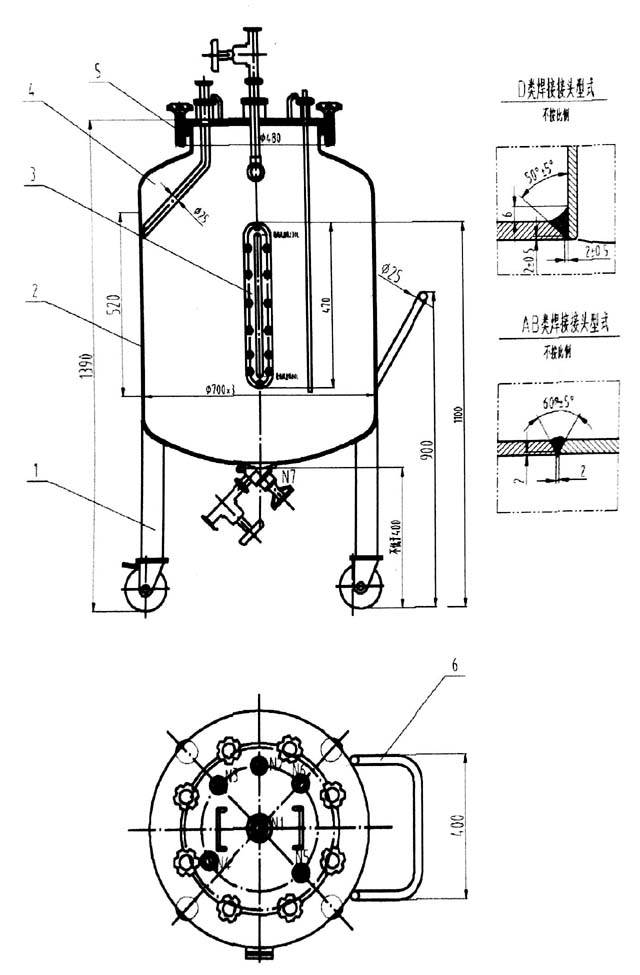
6.发布人名称:国药集团武汉血液制品有限公司
6.1联系地址:武汉市江夏区黄金工业园路一号附一号
6.2报名联系人:何欣宇
联系电话:027-86637222
报名邮箱:286131130@qq.com